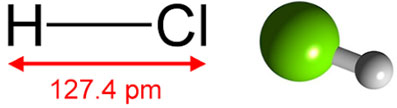
اسید هیدروکلریک یک ترکیب شیمیایی پرکاربرد است که از دو عنصر هیدروژن و کلر تشکیل شده است. این ترکیب زمانی که در آب حل می شود اسیدیته آب را کاهش می دهد و قبل از حل شدن در آب به عنوان کلرید هیدروژن شناخته می شود. بسیاری از صنایع جزو مصرف کنندگان اسید کلریدریک هستند.
خرید اسید هیدروکلریک
برای خرید آنلاین اسید هیدروکلریک با بهترین قیمت و تضمین کیفیت از بهترین برندهای موجود بازار از فروشگاه معتبر ایآز بازدید نمائید
فهرست مطالب
نگاهی به تاریخچه
اسید کلریدریک از همان ابتدای تاریخ پیدایش و مصرف، یک ماده شیمیایی مهم برای استفاده بوده است. هیدروکلریک اسید توسط شیمیدان معروف ایرانی، جابر بن حیان در حدود سال ۸۰۰ میلادی کشف شده است.
“Aqua regia”، مخلوطی متشکل از دو اسید کلریدریک و نیتریک است و از حل شدن “سال آمونیاک” در اسید نیتریک تهیه میشود؛ این روشها و ترکیبات در کارهای تحقیقاتی سودو-گبر (Pseudo-Geber)، شیمیدان اروپایی قرن سیزدهم شرح داده شد.
اسید کلریدریک آزاد برای اولین بار به طور عمومی در قرن شانزدهم توسط “لیباویوس” توصیف شد؛ او توانست این اسید را با حرارت دادن نمک در بوتههای سفالی تهیه کند.
برخی از منابع ادعا میکنند که کلریدریک اسید خالص برای اولین بار توسط راهب آلمانی در قرن پانزدهم کشف شد؛ هنگامی که او نمک معمولی و ویتریول سبز را حرارت داد. در حالی که سایر منابع معتقدند که هیچ اشاره روشنی به تهیه هیدروکلریک اسید خالص تا پایان قرن شانزدهم نشده است.
در قرن هفدهم، “یوهان رودولف گلاوبر” آلمانی، از نمک کلرید سدیم و اسید سولفوریک برای تهیه سولفات سدیم در فرآیند مانهایم استفاده کرد. در این فرآیند، گاز کلرید هیدروژن آزاد میشود.
جوزف پریستلی، دانشمند انگلیسی، هیدروژن کلرید خالص را در سال ۱۷۷۲ تهیه کرد. تا سال ۱۸۰۸ هامفری دیوی از انگلیس ثابت کرد که این ترکیب شیمیایی شامل هیدروژن و کلر است.
در طول انقلاب صنعتی در اروپا، تقاضا برای مواد قلیایی افزایش یافت. یک فرآیند صنعتی جدید که توسط “نیکلاس لبلانک” از فرانسه معرفی شد، تولید گسترده و ارزان کربنات سدیم را امکان پذیر کرد.
در این فرآیند، نمک معمولی با استفاده از اسید سولفوریک، سنگ آهک و زغال سنگ به سودا اَش تبدیل میشود و کلرید هیدروژن به عنوان محصول جانبی آزاد میشود.
تا قبل از اینکه روشهایی برای جمع آوری ترکیب HCl اضافی ارائه شود، این ماده در هوا آزاد میشد. در سال ۱۸۳۰، جذب HCl به این حوزه از صنعت معرفی شد. از اسید کلریدریک تولید شده، در ساخت “سال آمونیاک” (کلرید آمونیوم) استفاده شد.
در قرن ۲۰، فرآیند Leblanc به طور مؤثر با فرآیند Solvay جایگزین شد، بدون اینکه فرآورده جانبی این اسید تولید شود.
از آنجایی که کلریدریک اسید قبلاً به عنوان یک ماده شیمیایی مهم در کاربردهای فراوان شناخته شده بود، شرکتها روشهای تولید دیگری را آغاز کردند که برخی از آنها امروزه نیز مورد استفاده قرار میگیرند. بعد از سال ۲۰۰۰، هیدروکلریک اسید بیشتر از جذب کلرید هیدروژن که یک محصول جانبی از تولید ترکیبات آلی صنعتی است، تولید میشود.
جدول مشخصات فنی اسید کلریدریک
| فرمول مولکولی | HCl |
| جرم مولی | 36.46 g/mol |
| شکل ظاهری | مایع شفاف و بیرنگ تا زرد روشن |
| چگالی | 1.18 g/cm3 |
| انحلال پذیری در آب | کاملا محلول |
| نقطه ذوب | -85.05 °C |
روشهای تولید اسید هیدروکلریک (HCl)

اسید کلریدریک با روش های متعددی تولید می شود. اولین روش واکنش سوزاندن کلر در هیدروژن است. روش دوم واکنش اسید سولفوریک با کلرید سدیم است. در صنعت تولید اسید کلریدریک بدین صورت است که آن را از محصولات جانبی تولید می کنند مانند فرایند کلرزنی ترکیبات آلی.
از طریق هریک از این روش ها می توان انواع مختلفی از گریدهای اسید کلریدریک را تولید کرد. هیدروکلریک اسید کاملا خالص با استفاده از روش اول یا دوم تولید می شود و اسید کلریدریک صنعتی، که ناخالص تر است و مقدار کمی از ترکیبات آلی نیز در آن وجود دارد با استفاده از آخرین روش که کلرزنی ترکیبات آلی است بدست می آید.
در صنعت تولید اسید هیدروکلریک از واکنش مستقیم و به صورت چند مرحله ای انجام می شود. این روش به دلیل اینکه ناخالصی بسیار کمی دارد از کیفیت بالایی برخوردار است. این واکنش بسیار گرمازا است به این معنی که در طول مراحل تولید مقدار زیادی انرژی حرارتی آزاد می شود. به همین دلیل بهتراست یک خنک کننده نصب شود و اقدامات احتیاطی را رعایت کنید.
کاربردهای اسید کلریدریک
کاربردهای اسید هیدروکلریک بسیار زیاد است و در صنایع مختلف کاربردهای فراوانی دارد که در اینجا در مورد کاربردهای این اسید در هریک از صنایع را به شمامیگوییم.
کاربرد کلریدریک اسید در صنعت
یکی از کاربردهای کلریدریک اسید ، کاربرد این اسید در صنعت های مختلف است که میتوان به موارد زیر اشاره کرد:
..کاربرد اسید کلریدریک به عنوان اسیدشو در صنعت فولاد
یکی از مهمترین کاربردهای اسید کلریدریک ، استفاده از آن در اسید شویی فولاد است و برای رفع زنگ آهن روی آهن و فولاد استفاده میشود. در اسیدشویی فولادهای کربنی از HCL با غلظت 18 درصد استفاده میشود و این اسید با این غلظت در اسیدشویی رایج تر است.
صنایع اسیدشویی فولاد بهبودهای زیادی در بازسازی هیدروکلریک اسید ایجاد کرده است و برای تولید هیدروکلریک اسید از این روش نیز استفاده میشود.
..کاربرد کلریدریک اسید در تولید ترکیبات آلی
از دیگر کاربردهای این اسید ، کاربرد آن در تهیه و تولید ترکیبات آلی است مثل وینیل کلراید و دی کلرواتان برای پلی وینیل کلراید یا pvc است. محصولات آلی مثل کربن فعال و اسید اسکوربیک محصولاتی هستند که با استفاده از کلریدریک اسید تولید میشوند.
..کاربرد هیدروکلریک اسید در تولید ترکیبات غیر آلی
محصولات زیادی توسط هیدروکلریک اسید طی یک واکنش اسید و باز طبیعی منجر به ترکیبات معدنی (غیرآلی) تولید میشوند و هم چنین مواد شیمیایی درگیر با آب مثل کلرید آهن (III) و پلی آلومینیوم کلراید (PAC). واکنش آن هم به شکل زیر است:
Fe2O3 + 6 HCl → 2 FeCl3 + 3 H2O (کلرید آهن (III) از مگنتیت)
کلرید آهن (III) و PAC هر دو به عنوان عوامل لخته سازی و انعقاد در تصفیه آب و فاضلاب، تولید آب آشامیدنی و تولید کاغذ به کار میروند. دیگر ترکیبات معدنی تولید شونده با هیدروکلریک اسید شامل کلرید کلسیم، نمک پخش در جاده، کلرید نیکل (II) برای آبکاری الکتریکی و کلرید روی برای صنعت گالوانی کردن و تولید باتری هستند. در پایین واکنش کلرید کلسیم از سنگ آهک را برای شما می آوریم:
CaCO3 + 2 HCl → CaCl2 + CO2 + H2O
..کاربرد اسید کلریدریک در خنثی سازی و کنترل PH
از دیگر مزایای کلریدریک اسید خاصیت خنثی سازی و کنترل PH اسیدی موارد مختلف است.
..کاربرد هیدروکلریک اسید در سفیدکننده ها و مواد شیمیایی
یکی از کاربردهای جالب این اسید مزایای منحصر به فرد آن در خانه است که میتوان به مواردی مثل جوهر نمک و.. اشاره کرد. محلول های HCL در غلظت های پایین تر که خورندگی کمتری دارند برای تمیزکردن موادی مثل آهن، مس ، برنج و دیگر فلزات بکار میروند.
تفاوت وایتکس و جوهر نمک چیست؟
وایتکس از یک محلول قلیایی با نام شیمیایی سدیم هیپوکلریت تشکیل شده است و یک عامل اکسیداسیون قوی به شمار می رود. وقتی این ماده با هیدروکلریک اسید مخلوط می گردد سبب اکسید شدن اسید و آزاد سازی گاز کلر طبق واکنش زیر می شود
NaClO + 2 HCl —-> Cl2 + H2O + NaCl
نمک تولید شده از مخلوط این دو ماده خطرناک نیست اما کلر به محض اختلاط از محلول جدا می شود و به هوا منتشر می گردد. گاز کلر (chlorine gas) بسیار واکنش پذیر می باشد زیرا پیوند بین دو اتم کلر بسیار ضعیف است. میزان گاز کلر تولید شده به مقدار استفاده از این ماده و غلظت آن ها بستگی دارد اما به هیچ وجه توصیه نمی شود تا این دو ماده را با هم حتی در مقادیر کم نیز اختلاط نمایید.
..کاربرد این اسید در صنایع غذایی
کلریدریک اسید نیز در اسیدی کردن بعضی موادغذایی یا حتی برای نوآوری آنها استفاده میشود. از این اسید در فراوری مواد غذایی مثل: بیسکوییت ها، کراکر، سس گوجه و غلات استفاده میشود. اسید کلریدریک به عنوان اسیدی کننده برای طعم دهندگی و کاهش فساد در موادی مثل : کنسروها، آب سبزیجات و سس ها به کار میرود.
یکی از کاربردهای دیگر این اسید ، نقش مهمش در معده به عنوان اسید معده است که دارای PH حدودا 1 و نیم است.
.. اسید کلریدریک در جنگ و سلاح های شیمیایی
از خطرناکترین کاربردهای هیدروکلریک اسید ، کاربردش در سلاح های شیمیایی و استفاده آن در جنگ است که یکی از مرسوم ترین آن گاز خردل پخش شده با این سلاح است که دارای گوگرد و سمی است. معمولاً کشنده نیست، مگر اینکه قرار گرفتن در معرض این ماده با غلظت های بالا در فواصل منظم رخ دهد. این عامل تاول زا ،به پوست و غشاهای مخاطی دستگاه تنفسی و دستگاه گوارش حمله می کند و باعث سوختگی، تورم، تحریک و تاول های پر از چرک می شود. گاز خردل همچنین باعث جهش در DNA می شود و یک عامل سرطان زای شناخته شده است و هیچ پادزهری برای این ماده خطرناک وجود ندارد.
روش های متفاوتی برای تولید گازخردل وجود دارد که یکی از این روش ها استفاده از هیدروکلریک اسید است. البته یکی دیگر از گازهای سمی مورد استفاده در جنگ گاز فسژن است اما در تهیه آن کلریدریک اسید نقشی ندارد.
مزایای کلریدریک اسید
- پایدار است و غلظت خود را در طول زمان حفظ می کند.
- تمایل کمتری به شرکت در واکنش اکسایش کاهش دارد.
- ویژگی جرم گیری و ضد عفونی کنندگی
- محلول در آب
ایمنی هیدروکلریک اسید
حفاظت پوست : دستکش، لباس و کفش مقاوم در برابر مواد شیمیایی.
حفاظت چشم : محافظ صورت ضروری است.
حفاظت بدن : دستکش، لباس و کفش مقاوم در برابر مواد شیمیایی. دوش و چشم شور ایمنی در محیط های کار با این ماده الزامی است.
حفاظت تنفسی : از ماسک مناسب استفاده شود.
عوارض ناشی از تنفس این گاز
- تنگی قفسه سینه و احساس خفگی.
- لب ها و ناخن های شما آبی رنگ یشود.
- سرگیجه و فشار خون پایین از عوارض دیگر آن است.
- سرفه کردن خون و همینطور داشتن ضعف از عوارض تنفس هیدروکلریک است.
عوارض ناشی از تماس این اسید با پوست
- پوست دچار تاول زدگی میشود.
- داشتن احساس درد و سوزش
- در صورت تماس آن با چشم ممکن است بینایی خود را از دست دهید.
عوارض ناشی از استشمام یا مصرف تصادفی هیدروکلریک
- احساس سوزش در دهان و گلو
- دچار مشکلات تنفسی میشوید به دلیل متورم شدن گلو
- استفراغ خونین
- درد شدید شکم و قفسه سینه نیز از عوارض مصرف این اسید است.
بسته بندی اسید کلریدریک
خرید و فروش اسید کلریدریک در بسته بندیهای بشکهای از جنس پلاستیک – پلیمری انجام میگیرد. حجم این بشکهها عموماً ۲۲۰ لیتری است. امکان سفارش و خرید این اسید به صورت فلهای هم وجود دارد. تانکرهای ۲۵ تنی، برای حمل و نقل فلهای اسید استفاده میشوند.
مخازن این تانکرها از فولاد مقاوم به اسیدها ساخته شدهاند و روی آنها، علامت خورنده بودن اسید و علامت مخصوص حمل مواد شیمیایی خطرناک، درج شده است.
بسته بندیهای اسید کلریدریک در گرید آزمایشگاهی و با خلوص ۳۰ تا ۳۳ درصد، یا اسید کلریدریک ۳۷ درصد، در حجم ۵/۲ لیتر، ۵ لیتر و یا ۲۰ لیتر موجود است. هیدروکلریک اسید مرک و اسید سیگما آلدریچ، دو برند آزمایشگاهی برای این ترکیب هستند.
ذخیره سازی اسید کلریدریک
بشکههای حاوی هیدروکلریک اسید را باید در یک مکان خنک، خشک و دارای تهویه مناسب و به دور از مواد ناسازگار نگهداری کنید. انبار محل نگهداری اسید، یک منطقه با ماهیت خورنده است. این اسید را نباید در ظروف فلزی نگهداری کنید. کلرید هیدروژن را دور از مواد قلیایی نگهداری کنید. بشکهها و مخازن را از مواد اکسید کننده جدا نگه دارید.
بعد از کار کردن با اسید، دستان خود را کاملاً بشویید. برای حذف آلودگی، لباسها را قبل از استفاده مجدد، بشویید. محتویات بشکهها ممکن است در طولانی مدت دچار افزایش فشار داخلی شوند.
مواظب باشید اسید کلریدریک با چشم، پوست یا لباس شما تماس نداشته باشد. ظرف اسید را محکم و درب بسته نگه دارید.
بشکههای حاوی این اسید را در مجاورت بازها و فلزات نگهداری نکنید. هنگام باز کردن درب بشکهها باید بسیار احتیاط کنید.
از پیمانههای فلزی یا سایر وسایل فلزی برای برداشتن حجمی از اسید، استفاده نکنید. بخار یا غبار کلریدریک اسید را تنفس نکنید. فقط در صورتیکه انبار، تهویه مناسب دارد یا ماسک تنفسی مناسب دارید، از آن استفاده کنید.
وضعیت بازار و خرید و فروش و قیمت روز اسید کلریدریک
بازار خرید و فروش اسید کلریدریک بسیار پرتقاضا است. تولید هیدروژن کلرید در طول سال، میلیونها تن است که علاوه بر تأمین نیاز بازار داخلی، برای صادرات هم در نظر گرفته میشود. اسید هیدروکلریک، ترکیبی است که بسیاری از فرآیندهای صنعتی به آن وابسته است.
فروش اسید کلریدریک ۳۳%، اسید کلریدریک ۳۷%، یا کلریدریک اسید ۳۰%، در بسته بندیهای استاندارد و مطابق با نیاز مشتری انجام میشود. هیدروژن کلرید، یک ترکیب قطبی است و به این جهت بسیار واکنش پذیر است. به همین دلیل، حمل و نقل آن باید با رعایت تمام استانداردهای ایمنی و کار با مواد شیمیایی خطرناک و خورنده انجام گیرد.
قیمت اسید کلریدریک با توجه به ترکیبات اولیه برای تولید و میزان عرضه و تقاضا در بازارهای داخلی و بازار جهانی تعیین میشود.

