اسید سولفامیک یا سولفامیک اسید یک ترکیب جامد پودری سفید رنگ با فرمول مولکولی (H3NSO3) و دارای ذرات ریز و کریستالی درخشان می باشد. سولفامیک اسید یک اسید نسبتا قوی است که به راحتی می تواند نمک سولفامات را تشکیل دهد.
اسید سولفامیک محلول در آب بوده و با نام های دیگری نظیر آمیدو سولفوریک اسید، آمیدو سولفونیک اسید، آمینو سولفونیک و اسید سولفامیدیک نیز شناخته می شود.
در برخی موارد این اسید قوی به عنوان جایگزینی برای اسید کلریدریک(هیدروکریک) در کاربردهای تمیزکنندگی مورد استفاده قرار می گیرد.
خرید اسید سولفامیک
برای خرید آنلاین اسید سولفامیک با بهترین قیمت و تضمین کیفیت از بهترین برندهای موجود بازار از فروشگاه معتبر ایآز بازدید نمائید
فهرست مطالب
1.ساختار اسید سولفامیک
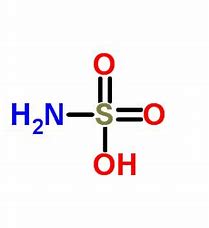
از نظر ساختار شیمیایی، اسید سولفامیک به عنوان ترکیب واسط بین اسید سولفوریک و سولفامید قرار دارد. ترکیبات سولفامات نیز از مشتقات اسید سولفامیک هستند. این اسید جزو ساده ترین اسیدهای سولفامیک است که متشکل از یک اتم گوگرد منفرد می باشد. این گوگرد توسط پیوند کووالانسی با گروه های هیدروکسید و آمینه و توسط پیوندهای دوگانه به دو اتم اکسیژن متصل شده است.
2.جدول مشخصات فنی اسید سولفامیک

3.روش تولید و سنتز اسید سولفامیک
اسید سولفامیک (اسید آمیدوسولفوریک) یک اسید تک پایه، معدنی و خشک است که به شکل کریستالی تولید می شود.
اسید سولفامیک برای اولین بار در سال 1834 توسط شیمیدان آلمانی یوهان فریدریش دیلدرف (Johann Friedrich Dieldorff) سنتز شد. او اوره را با اسید سولفوریک واکنش داد و اسید سولفامیک تولید کرد.
NH2CONH2 + H2SO4 → H3NSO3 + NH4HSO4
این واکنش به نام واکنش دیلدرف شناخته می شود.
در سال 1844، شیمیدان انگلیسی ویلیام هیل (William Hill) یک روش جدید برای سنتز اسید سولفامیک توسعه داد. او اوره را با دی اکسید گوگرد واکنش داد و اسید سولفامیک تولید کرد.
NH2CONH2 + SO2 → H3NSO3
این روش امروزه به طور گسترده برای تولید اسید سولفامیک استفاده می شود.
محلول های آبی اسید سولفامیک به عنوان اسیدهای قوی مشابه اسید کلریدریک و اسید سولفوریک رتبه بندی می شوند
4.کاربردهای اولیه اسید سولفامیک
در اوایل قرن بیستم، اسید سولفامیک به عنوان یک ماده ضد رسوب در تولید کاغذ استفاده شد. این ترکیب می تواند رسوبات معدنی را در خمیر کاغذ حل کند و باعث بهبود کیفیت کاغذ شود.
اسید سولفامیک همچنین به عنوان یک عامل کاهنده در تولید رنگدانه ها استفاده شد. این ترکیب می تواند رنگدانه های رنگی را تولید کند.

5.کاربردهای مدرن اسید سولفامیک
امروزه اسید سولفامیک در صنایع مختلف کاربرد دارد. از جمله کاربردهای این ترکیب می توان به موارد زیر اشاره کرد:
- تولید کاغذ: اسید سولفامیک به عنوان یک ماده ضد رسوب در تولید کاغذ استفاده می شود. این ترکیب می تواند رسوبات معدنی را در خمیر کاغذ حل کند و باعث بهبود کیفیت کاغذ شود.
- تولید رنگدانه ها: اسید سولفامیک به عنوان یک عامل کاهنده در تولید رنگدانه ها استفاده می شود. این ترکیب می تواند رنگدانه های رنگی را تولید کند.
- تولید مواد شیمیایی: اسید سولفامیک به عنوان یک ماده اولیه برای تولید سایر مواد شیمیایی مانند سولفات آمونیوم، سولفات سدیم و سولفات آهن استفاده می شود.
- تصفیه آب: اسید سولفامیک برای تصفیه آب از فلزات سنگین مانند مس، نیکل و سرب استفاده می شود. این ترکیب می تواند این فلزات را از آب جدا کند.
- تمیز کردن و جرم زدایی: اسید سولفامیک به عنوان یک عامل جرم زدا برای تمیز کردن سطوح مختلف مانند سطوح فلزی، شیشه ای و پلاستیکی استفاده می شود. این ترکیب می تواند رسوبات و جرم های چسبیده به سطوح را از بین ببرد.این ترکیب برای سطوح سخت مانند صفحه دوش، کاشی، شیرآلات، سینک ظرفشویی، توالت، حمام، آبگرم و نیمکت هایی که از اکریلیک، کروم، فولاد ضد زنگ، سرامیک و فایبرگلاس ساخته شده است و در حمام، آشپزخانه و غیره استفاده می شود، بی خطر است. اسید سولفامیک نباید روی سطوح مرمر استفاده شود.
6.بسته بندی و شرایط نگهداری اسید سولفامیک
- اسید سولفامیک مایع، پودری، در ظروف دربسته و در مکانی خشک و خنک نگهداری کنید.دمای نگهداری مطلوب بین 15 تا 25 درجه سانتیگراد است. اسید سولفامیک باید دور از نور خورشید و منابع گرما نگهداری شود.
- این مواد را می توان طولانی مدت در ظروف آزمایشگاهی، پاکت های پلاستیکی یا الیافی نگهداری کرد.
- اسید سولفامیک را در مکانی با تهویه مناسب و دور از نور خورشید نگه دارید.
- سولفامیک اسید در بسته بندی های ۱ کیلوگرم | ۵ کیلوگرم | ۱۰ کیلوگرم به فروش می رسد.
7.مزایای استفاده از اسید سولفامیک
- ماندگاری بسیار بالایی دارد.
- دارای اثر بسیار بالایی در رسوب زدایی است.
- می تواند مستقیما به سیستم وارد شود و هزینه سیستم را کاهش می دهد.
- می توان با استفاده از اسید سولفامیک از نظر شیمیایی تمیزکاری را بطور کامل انجام داد و نیازی به اقدامات بعدی ندارد.
- در هیچ سیستمی نیازمند تعیین دوز نیست.
- برای رسوب زدایی از کندانسور در حال اجرا توصیه می شود که آن را به آب خنک کننده اضافه کنید.
- یک اسید بی خطر است و در صورت استفاده از تجهیزات ایمنی هیچ خطری برای سلامتی ندارد.
8.ارتباط اسید سولفامیک با سولفامات ها
9.اسید سولفامیک می تواند جایگزین چه مواد شیمیایی باشد؟
سولفامیک اسید می تواند جایگزین مواد شیمیایی زیر باشد:
- اسید سولفوریک (H2SO4): سولفامیک اسید یک جایگزین ملایم تر از اسید سولفوریک است که می تواند در کاربردهایی که نیاز به اسید قوی نیست، استفاده شود. به عنوان مثال، سولفامیک اسید می تواند برای تولید اسیدهای معدنی ضعیف تر مانند سولفات آمونیوم استفاده شود.
- اسید سیتریک (C6H8O7): سولفامیک اسید می تواند به عنوان یک جایگزین برای اسید سیتریک در کاربردهایی مانند تولید مواد شوینده و محصولات آرایشی بهداشتی استفاده شود.
- اسید فسفریک (H3PO4): سولفامیک اسید می تواند به عنوان یک جایگزین برای اسید فسفریک در کاربردهایی مانند تولید کودها و مواد رنگی استفاده شود. با این حال، لازم به ذکر است که سولفامیک اسید همیشه یک جایگزین مناسب برای مواد شیمیایی دیگر نیست. در برخی موارد، ممکن است لازم باشد از مواد شیمیایی خاص برای دستیابی به خواص مورد نظر استفاده شود
10.نکات ایمنی اسید سولفامیک
اسید سولفامیک یک ترکیب شیمیایی سمی است و باید با احتیاط استفاده شود. تماس این ترکیب با پوست و چشم می تواند باعث تحریک و سوختگی شود. همچنین، استنشاق بخارات این ترکیب می تواند باعث تحریک دستگاه تنفسی شود.
در هنگام کار با اسید سولفامیک باید از تجهیزات ایمنی مانند دستکش، عینک ایمنی و ماسک استفاده شود. همچنین، باید از تماس این ترکیب با پوست، چشم و دستگاه تنفسی خودداری شود.

11.اثرات قرار گرفتن طولانی مدت در معرض اسید سولفامیک
در غلظت های پایین: می تواند باعث خشکی، قرمز شدن و ترک خوردن پوست (درماتیت) در پی تماس با پوست شود.
در غلظت های بالا: ممکن است مینای دندان را هنگام تنفس از بین ببرد. ممکن است به سیستم تنفسی آسیب برساند. می تواند مجاری تنفسی را تحریک و ملتهب کند.
سرطان زایی: مشخص نیست که باعث سرطان می شود ولی غیر آلی قوی حاوی سولفوریک اسید برای انسان سرطان زا هستند. در برخی تحقیقات ارتباط آن با سرطان حنجره، سرطان ریه مشاهده شده است.

12.بازار جهانی اسید سولفامیک
بازار جهانی اسید سولفامیک در سال 2022 ارزشی معادل 375 میلیون دلار داشت و پیش بینی می شود تا سال 2031 به ارزش 1.4 میلیارد دلار برسد. این رشد 15 درصدی در طی دوره 10 ساله بین سال های 2022 تا 2031 را نشان می دهد.
تقاضا برای اسید سولفامیک در صنایع مختلف در حال افزایش است. این امر به دلیل مزایای متعدد این ترکیب شیمیایی مانند قیمت پایین، سمیت کم و کاربردهای متنوع است.
رشد تقاضا برای اسید سولفامیک در صنایع مختلف باعث افزایش تولید این ترکیب شیمیایی در سراسر جهان شده است. در حال حاضر، کره جنوبی، چین و ایالات متحده سه تولیدکننده برتر اسید سولفامیک در جهان هستند.
با توجه به رشد تقاضا برای اسید سولفامیک در صنایع مختلف، پیش بینی می شود این ترکیب شیمیایی همچنان به عنوان یک محصول مهم در بازار جهانی باقی بماند.







