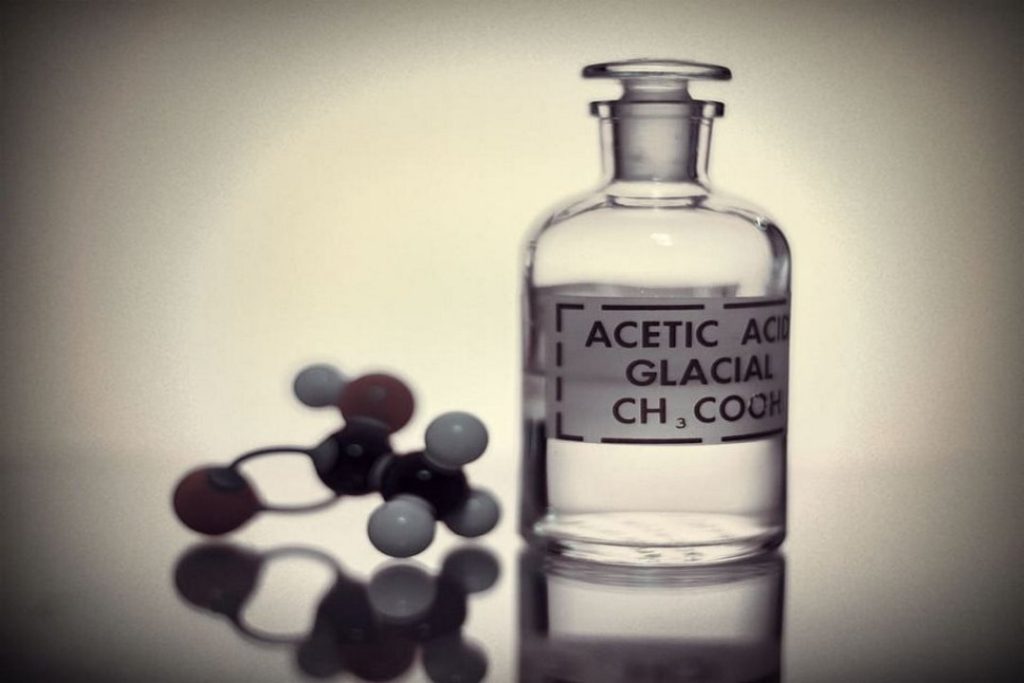
رابطه ی عمیقی که شیمی با زندگی روزمره ی انسان ها دارد، روزبه روز گسترده تر می شود؛ اسید استیک یک مثال عالی برای این رابطه است. این ماده، مایعی شفاف با بوی تند و تیز است که به شکل سنتی آن را به نام سرکه می شناسند. این ماده ی شیمیایی رایج در جهان تقاضای بسیار بالایی دارد. تقریبا سالیانه 15 میلیون تن از این ماده برای کاربردهای صنعتی شیمیایی و غذایی تولید می شود. به همین دلیل روش های تهیه اسید استیک دسته بندی بسیار وسیعی را در بر می گیرد. خرید اسید استیک توسط صنایع مختلف از جمله شیمیایی، دارویی، پلیمر، رنگ، غذایی و مواد افزودنی انجام می شود. با توجه به تقاضای روز افزون برای این ماده پیش بینی می شود تولید آن رشد 5 درصدی داشته باشد و به سالیانه 18 میلیون تن برسد.
خرید اسید استیک
برای خرید آنلاین اسید استیک با بهترین قیمت و تضمین کیفیت از بهترین برندهای موجود بازار از فروشگاه معتبر ایآز بازدید نمائید
فهرست مطالب
اسید استیک چیست؟
اسید استیک به خانواده کربوکسیلیک اسید تعلق دارد و از آن در صنعت یا در مواد خوراکی مانند سرکه استفاده میشود. اسید استیک با نامهای دیگری مانند اتانوییک اسید یا جوهر سرکه شناخته میشود و در دسته اسیدهای ضعیف قرار میگیرد. البته با وجود اینکه این اسید قدرت بالایی ندارد اما در صورتیکه غلظت آن بالا باشد میتواند برای ریه، چشمها، بینی و گلو خطرناک باشد. در این مطلب برای اینکه بیشتر با استیک اسید آشنا شوید به ساختار، خواص فیزیکی و شیمیایی آن ازجمله pH، روش تولید،کاربرد،بسته بندی و همچنین رعایت نکات ایمنی به هنگام استفاده از این اسید میپردازیم.
ساختاراسید استیک
ساختار استیک اسید مانند ساختار کلی کربوکسیلیک اسید ها می باشد، در واقع از یک گروه متیل متصل به یک گروه کربوکسیل تشکیل شده است. در اسید استیک جامد، مولکول ها زنجیره هایی را تشکیل می دهند و مولکول های جداگانه توسط پیوندهای هیدروژنی به هم متصل می شوند.

تاریخچه اسید استیک
سرکه در همان تمدنهای اولیه به عنوان محصول طبیعی واکنشهای هوازی نوشیدنی الکلی شناخته میشد، زیرا باکتریهای تولید کننده اسیداستیک در همه محیطها وجود دارند. استفاده از استیک اسید در شیمی تا قرن ۳ پیش از میلاد گسترش یافت؛ زمانی که فیلسوف یونانی “تئوفراستوس”، نحوه اثرگذاری سرکه بر روی فلزات را برای تولید رنگدانه های کاربردی (= از جمله کربنات سرب، مخلوط سبز نمکهای مس) توصیف کرد.
در قرن شانزدهم، شیمیدان آلمانی، “آندریاس لیباویوس” تولید استون را از تقطیر خشک استات سرب، روشن “دکربوکسیلاسیون کتونیک” ارائه کرد. وجود آب در سرکه تأثیرات زیادی در خصوصیات اسید استیک میگذارد؛ چیزی که باعث شد برای قرنها، شیمی دانان معتقد باشند که اسید استیک یخی و اسید موجود در سرکه دو ماده متفاوت هستند. “پیر آدت” شیمیدان فرانسوی ثابت کرد که هر دو ترکیب، یکسان هستند.
در سال ۱۸۴۵، شیمی دان آلمانی، “هرمان کولبه” برای اولین بار، استیک اسید را از ترکیبات غیر آلی سنتز کرد. این توالی واکنش شامل کلراسیون دی سولفید کربن به تتراکلرید کربن؛ و به دنبال آن، پیرولیز تتراکلرواتیلن و کلریناسیون محلول آبی اسیدتری کلرواستیک است که در اثر تجزیه الکترولیتی، به اتانوئیک اسید ختم میشود. تا سال ۱۹۱۰، بیشترین اسید استیک گلاسیال، از تقطیر چوب، به دست آمد.
مشخصات فنی اسید استیک
| نام شیمیایی | اسید استیک | Acetic acid |
| فرمول ساختاری | CH3COOH یا C2H4O2 |
| نقطه ذوب و نقطه انجماد | 16.6 درجه سانتیگراد( محلول 100٪) |
| وزن مولکولی | 60.05 g/mol |
| نقطه جوش | 118 درجه سانتی گراد |
| شکل ظاهری | شفاف و بی رنگ |
ویژگیهای فیزیکی و شیمیایی اسید استیک
اسید استیک، یک اسید ضعیف با فرمول مولکولی CH3COOH و وزن مولکولی 60.05 گرم بر مول، جزو مواد معدنی و متعلق به گروه اسیدهاست که به صورت مایعی بیرنگ و بویی مشابه سرکه دارد. این ماده قابل اشتعال، قدرت خورندگی بسیار بالایی دارد و همچنین در دمای 16.6 درجه سانتیگراد منجمد میشود.
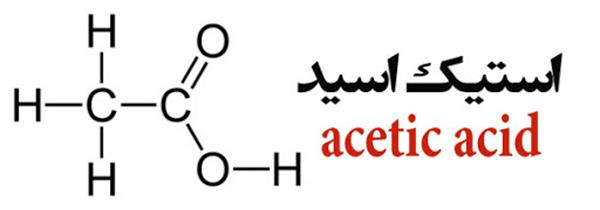
نقطهی جوش این اسید 117.9 درجه سانتیگراد و نقطهی ذوب آن 61.9 درجه سانتیگراد است. سادهترین کربوکسیلیک اسید بعد از فرمیک اسید به شمار میرود. این اسید در آب انحلالپذیر است و به طور کامل در آب مخلوط میشود. اسید استیک مادهای قطبی بوده و با نام اختصاری AcOH نیز نشان داده میشود. در سرکههای خوراکی، تقریبا 4 تا 8 درصد وزنی استیک اسید وجود دارد.
این ماده در صنعت و بازار فروش آن با نامهای دیگری از جمله اسید اتانوئیک، متان کربوکسیلیک اسید و سرکه شناخته میشود.
فرآیند تولید اسید استیک
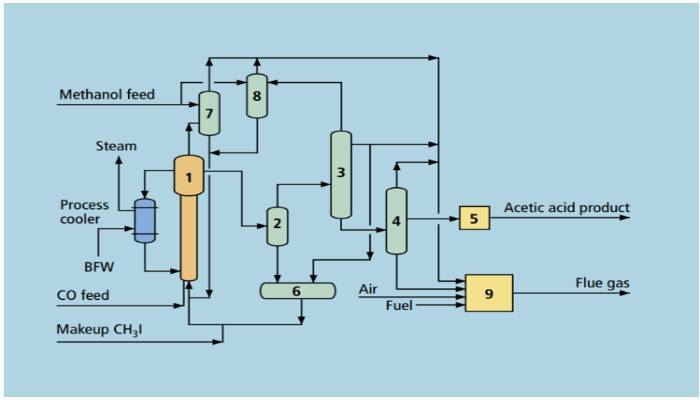
سنتز اسید استیک
اسید استیک به دو روش مصنوعی (کربونیلاسیون متانول) و یا بیولوژیکی (تخمیر باکتریایی) تولید می شود. 75 درصد استیک اسید مورد استفاده در صنایع شیمیایی از کربونیلاسیون متانول تهیه می شود و مسیر بیولوژیکی فقط 10 درصد از تولید جهانی را شامل می شود.
1_روش های بیولوژیکی تولید اسید استیک
تخمیر هوازی: در تخمیر هوازی محلول رقیق الکل با استوباکتر مخلوط شده و در مکان گرم و آرام نگهداری می شود و طی چند ماه الکل به سرکه تبدیل می شود. در این روش با بهینه سازی تزریق اکسیژن به باکتری ها این روند تسریع می شود. در صورت وجود اکسیژن کافی این باکتری می تواند از انواع مختلف غذاهای الکل دار مانند سیب، شراب، مالت، برنج و سیب زمینی سرکه تولید کند.
تخمیر بی هوازی: در این روش برخی از گونه های باکتری های بی هوازی می توانند قندها را مستقیما به اسید استیک تبدیل کنند بدون اینکه اتانول به عنوان واسطه ایجاد شود. این باکتری ها می توانند اسید استیک را از ترکیبات یک کربنه از جمله متانول، مونوکسید کربن و یا مخلوطی از دی اکسید کربن و هیدروژن تولید کنند.
2_روش های صنعتی تولید اسید استیک
فرآیند کربونیلاسیون: در این فرآیند متانول و مونو اکسید کربن در فشار بالا با هم واکنش می دهند و استیک اسید تهیه می شود.
اکسیداسیون استالدئید: در این روش استالدئید را می توان با اکسیژن هوا در حضور کاتالیزور های فلزی مانند نمک های کبالت و کروم اکسید کرد و اسید استیک تهیه کرد. در این واکنش محصولات جانبی اتیل استات، اسید فرمیک و فرمالدئید به وجود می آید که همه آنها دارای نقاط جوش پایین تر از اسید استیک هستند و به راحتی با تقطیر جدا می شوند.
اکسیداسیون بوتان: در این واکنش بوتان به راحتی با اکسیژن هوا در حضور کاتالیزور های فلزی اکسید شده و به پراکسید تبدیل می شود و سپس پراکسید تجزیه شده و اسید استیک به دست می آید.
کاربردهای اسید استیک
از جمله کاربردهای اسید استیک به موارد زیر اشاره می شود:
- تولید مونومر وینیل استات
- تولید سرکه خانگی
- در تولید نفت
- به عنوان پیش ماده پلی استیل و استات سلولزی
- برای تبلور مجدد برای خالص سازی ترکیبات آلی
- تولید نمک های آلی یا غیر آلی
- معرف شیمیایی مهم برای تولید ترکیبات شیمیایی
- تولید استات سلولز برای فیلم عکاسی
- به دلیل خاصیت ضد باکتریایی برای تولید ضد عفونی کننده
- استات پلی وینیل برای چسب چوب
- اسید استیک در رنگرزی مصرف می شود.
- تولید الیاف مصنوعی و پارچه ها
- تولید لاستیک
- در کشاورزی به عنوان علف کش و از بین برنده علف های هرز
- در تولید مواد رسوب زدایی
- در آماده سازی صنعتی دی متیل ترفتالات (DMT)
- درعلم پزشکی برای درمان سرطان با تزریق مستقیم آن به تومور
- در متابولیسم کربوهیدرات ها و چربی ها نقش بسزایی دارد.
- در صنایع غذایی، به عنوان تنظیم کننده اسیدیته و چاشنی با کد افزودنی غذایی E260 کاربرد دارد.
بسته بندی و شرایط نگهداری اسید استیک
اسید استیک در ظروف آلومینیومی و شیشه ای و یا در ظروف پلاستيكی ( پلی اتيلنی سنگين) دارای برچسب مخصوص و مناسب نگهداری می شود. از نگهداری آن در ظروف فولادی، آهنی، روی، سربی، مسی و برنز خودداری شود .
از جمله نکات مهم در شرایط نگداری اسید استیک، آن است که این ماده در محیط خشک و به دور از نور مستقیم آفتاب محافظت شود. درب ظرف باید کاملا پلمپ باشد، به گونه ای که در مقابل سرما محافظت شود. تانک نگهدارنده استیک اسید باید با سیم به زمین جهت تخلیه الکتریکی متصل باشد و تنها در مقادیر محدود آن را ذخیره کنید. در انبارهای نگهداری آن باید از تجهیزات ضد انفجار و ضد جرقه استفاده کرد.

انبار نگهداری اسید استیک

ظروف نگهداری اسید استیک
بازار خرید و فروش جهانی
اسید استیک در صنایع متنوعی از جمله منسوجات، مواد غذایی و نوشیدنی، کشاورزی، مواد تمیز کننده خانگی، پلیمرها، رنگ ها و پوشش ها کاربرد دارد. بر همین اساس ارزش بازار جهانی این ماده در سال 2022 برابر با 19.76 میلیارد دلار بوده است و پیش بینی می شود تا سال2032 به 32.65 میلیارد دلار برسد و نرخ رشد 5.2% را طی کند. بازار این ماده را بر اساس منطقه ی جغرافیایی می توان به بخش های گسترده ای تقسیم نمود. برای مثال آسیا به دلیل کاربرد در طیف گسترده ای از صنایع به شدت در رشد بازار این ماده موثر بوده است. به ویژه به دلیل کشورهای روبه توسعه مانند چین. از سوی دیگر آمریکای شمالی به دلیل تاثیر گسترده در بخش منسوجات، در بازار این ماده تاثیر گذار بوده است.
موارد ایمنی اسید استیک
اسید استیک غلیظ برای پوست، خورنده است. این سوختگیها یا تاولها ممکن است تا ساعتها پس از قرار گرفتن در معرض اسید، روی بدن وجود داشته باشند. اسید استیک گلاسیال به شدت خطرناک است.
استنشاق طولانی مدت (= حدود هشت ساعت) بخارات این ماده با غلظت ۱۰ ppm میتواند باعث تحریک چشم، بینی و گلو شود. در ۱۰۰ ppm، موجب تحریک شدید ریهها شده و ممکن است آسیب به سیستم تنفسی، چشمها و پوست ایجاد کند.
غلظت اسید در حالت بخار، ۱۰۰۰ ppm باعث تحریک چشم، بینی و دستگاه تنفسی فوقانی میشود و قابل تحمل نیست.
قرار گرفتن در معرض ppm 50 یا بیشتر از اسید استیک برای اکثر افراد قابل تحمل نیست و منجر به تحریک شدید چشم، بینی و گلو، همراه با برونشیت مزمن میشود. بسیاری از تحریکها برای سیستم پوست، بینایی و تنفسی است.
به شدت توصیه میشود که کارگران و افرادی که با این اسید سروکار دارند، لباس کار، عینک، ماسک و دستکش ایمنی استفاده کنند.
جمع بندی
به طور کلی اسیداستیک، اسیدی ضعیف و قابل اشتعال است که به دلیل خواص خود در صنایع مختلف کاربرد های گوناگونی را بر عهده گرفته است. این ترکیب آلی که به صورت مایع بی رنگ با بوی تند شبیه به سرکه است در صنایع غذایی، پزشکی، رنگ و غیره به کار برده می شود.

